Аминокислоты (далее по тексту — «А.») — это класс органических соединений, объединяющих в себе свойства кислот и аминов, т. е. содержащих наряду с карбоксильной группой — COOH аминогруппу — NH2. В зависимости от положения аминогруппы относительно карбоксильной группы различают ?-, ?-, ?- и др. А.
Рис. Наиболее сложными биополимерами являются белки. Их макромолекулы состоят из мономеров, которыми являются аминокислоты. Каждая аминокислота имеет две функциональные группы: карбоксильную и аминогруппу. Все разнообразие белков создается в результате различных сочетаний 20 аминокислот.
А. играют очень большую роль в жизни организмов, т. к. все белковые вещества построены из А. Все белки при полном гидролизе (расщеплении с присоединением воды) распадаются до свободных аминокислот, играющих роль мономеров в полимерной белковой молекуле. При биосинтезе белка порядок, последовательность расположения А. задаются генетическим кодом, записанным в химической структуре дезоксирибонуклеиновой кислоты. 20 важнейших А., входящих в состав белков, отвечают общей формуле RCH(NH2)COOH и относятся к ?-аминокислотам.
В природе встречаются и ?-аминокислоты., RCH(NH2)CH2COOH, например ?-аланин CH2NH2CH2COOH, входящий в состав пантотеновой кислоты. А. могут содержать одну NH2-группу и одну СООН-группу (моноаминокарбоновые кислоты), одну NH2-группу и две СООН-группы (моноаминодикарбоновые кислоты), две NH2-группы и одну СООН-группу (диаминомонокарбоновые кислоты).
Моноаминокарбоновые кислоты:
- Глицин — NH2CH2COOH
- Аланин — CH3CH (NH2) COOH
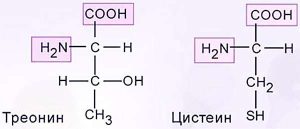
- Цистеин — CH2(SH)CH(NH2)COOH
- Метионин — CH2 (SCH3) CHмCH (NH2) COOH
- Валин-(СН3)2СНСН(МН2)СООН и др.
Моноаминодикарбоновые кислоты:
- Аспарагиновая — HOOC CHмCH (NH2) COOH
- Глутаминовая — HOOC (CH2)2CH (NH2) COOH
Диаминомонокарбоновые кислоты:
- Лизин — NH2CH2(CH3)2CH(NH2)COOH
- Аргинин — NH2C(=NH)NH(CH2)3CH(NH2)COOH и др.
Аминокислоты — бесцветные кристаллические вещества, растворимые в воде; их температура плавления составляет 220 — 315°С. Высокая температура плавления связана с тем, что их молекулы имеют структуру главным образом амфотерных (двузарядных) ионов. Например, строение простейшей аминокислоты — глицина — можно выразить формулой (а не NH2CH2COOH).
Все природные А., кроме глицина, содержат асимметричные атомы углерода, существуют в оптически активных модификациях и, как правило, относятся к L-ряду. Аминокислоты D-ряда содержатся только в некоторых антибиотиках и в оболочках бактерий.
Многие растения и бактерии могут синтезировать все необходимые им А. из простых неорганических соединений. Большинство А. синтезируются в теле человека и животных из обычных безазотистых продуктов обмена веществ и усвояемого азота. Однако 8 аминокислот (валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин) являются незаменимыми, т. е. не могут синтезироваться в организме животных и человека, и должны доставляться с пищей.
Суточная потребность взрослого человека в каждой из незаменимых аминокислот составляет в среднем около 1 г. При недостатке этих А. (чаще триптофана, лизина, метионина) или в случае отсутствия в пище хотя бы одной из них невозможен синтез белков и многих других биологически важных веществ, необходимых для жизни. Гистидин и аргинин синтезируются в животном организме, но лишь в ограниченной, иногда недостаточной, мере. Цистеин и тирозин образуются лишь из своих предшественников — соответственно метионина и фенилаланина — и могут стать незаменимыми при недостатке этих А. Некоторые А. могут синтезироваться в животном организме из безазотистых предшественников при помощи процесса переаминирования, т. е. переноса аминогруппы с одной аминокислоты на др.
В организме А. постоянно используются для синтеза и ресинтеза белков и других веществ — гормонов, аминов, алкалоидов, коферментов, пигментов и др. Избыток аминокислоты подвергается распаду до конечных продуктов обмена (у человека и млекопитающих до мочевины, двуокиси углерода и воды), при котором выделяется энергия, необходимая организму для процессов жизнедеятельности. Промежуточным этапом такого распада является обычно дезаминирование (чаще всего окислительное).
К числу производных А., представляющих большой практический интерес, относится лактам ?-аминокапроновой кислоты — исходный продукт производства капрона.
Известно много методов синтеза аминокислот, например действие аммиака на галогензамещённые карбоновые кислоты:
RCHCICOOH+2NH3 ? RCHNH2COOH + NH4CI,
восстановление оксимов или гидразонов, кето- или альдегидокислот:
RC(= NOH)COOH ? RCHNH2COOH
и др.
Некоторые А. выделяют из продуктов гидролиза богатых ими белков методом адсорбции на ионообменных смолах; так выделяют глутаминовую кислоту из казеина и клейковины злаков; тирозин — из фиброина шёлка; аргинин — из желатины; гистидин из белков крови. Некоторые А. производят синтетически, например метионин, лизин и глутаминовую кислоту. А. получают в больших количествах также микробиологическим синтезом. Поступление в организм незаменимых аминокислот определяется количеством и аминокислотным составом пищевых белков. Это следует учитывать для организации правильного общественного питания и составления рационов для разных возрастных и профессиональных групп населения. Потребность в пищевом белке может быть полностью покрыта за счёт смеси А. Этим пользуются в лечебном питании.
А. применяют в медицине: для парентерального питания больных (т. е. минуя желудочно-кишечный тракт) с заболеваниями пищеварительных и других органов, а также для лечения заболеваний печени, малокровия, ожогов (метионин), язв желудка (гистидин), при нервно-психических заболеваниях (глутаминовая кислота и т. п.); в животноводстве и ветеринарии — для питания (см. ниже) и лечения животных, а также в микробиологической, медицинской и пищевой промышленности.
Изучение аминокислотного состава белков и обмена А. проводят рядом цветных реакций, например нингидриновой реакцией, а также методами хроматографии и с помощью специальных автоматических приборов — анализаторов А.
Аминокислоты в кормлении сельскохозяйственных животных
Рационы с.-х. животных должны содержать все необходимые организму аминокислот, особенно незаменимые, поэтому при организации кормления в настоящее время стали учитывать в кормах не только общее количество протеина, как было принято раньше, но и незаменимых А. Потребность в А. у разных видов животных неодинакова. У жвачных животных микрофлора преджелудков способна синтезировать все необходимые организму А. из аммиака, выделяющегося при распаде белка или небелковых азотистых соединений, например мочевины. Нормирования А. для этих животных не проводят. Однако с целью пополнения рациона животных небелковыми азотистыми веществами применяют мочевину.
Молодняк жвачных, у которого ещё недостаточно развиты преджелудки, испытывает некоторую потребность в незаменимых аминокислотах Рационы свиней и птицы обязательно балансируют по содержанию А. С этой целью подбирают корма, дополняющие друг друга по аминокислотному составу, а также используют синтетические А., выпускаемые промышленностью.
Синтетические А. скармливают в смеси с концентратами; целесообразнее добавлять их в комбикорма промышленного изготовления.
Избыток аминокислот отрицательно влияет на организм животных. (И. Б. Збарский, Я. Ф. Комиссаров)
Открытие аминокислот в составе белков
| Аминокислота | Аббреви-атура | Год | Источник | Кто впервые выделил |
| Глицин | Gly, G | 1820 | Желатин | Анри Браконно |
| Лейцин | Leu, L | 1820 | Мышечные волокна | А. Браконно |
| Тирозин | Tyr, Y | 1848 | Казеин | Ф. Бопп |
| Серин | Ser, S | 1865 | Шёлк | Э. Крамер |
| Глутаминовая кислота | Glu, E | 1866 | Растительные белки | Г. Риттхаузен |
| Глутамин | Gln, Q | |||
| Аспарагиновая кислота | Asp, D | 1868 | Конглутин, легумин (ростки спаржи) | Г. Риттхаузен |
| Аспарагин | Asn, N | 1806 | Сок спаржи | Л.-Н. Воклен и П. Ж. Робике |
| Фенилаланин | Phe, F | 1881 | Ростки люпина | Э. Шульце, Й. Барбьери |
| Аланин | Ala, A | 1888 | Фиброин шелка | Т. Вейль |
| Лизин | Lys, K | 1889 | Казеин | Э. Дрексель |
| Аргинин | Arg, R | 1895 | Вещество рога | С. Гедин |
| Гистидин | His, H | 1896 | Стурин, гистоны | А. Кессель, С. Гедин |
| Цистеин | Cys, C | 1899 | Вещество рога | К. Мёрнер |
| Валин | Val, V | 1901 | Казеин | Герман Эмиль Фишер |
| Пролин | Pro, P | 1901 | Казеин | Э. Фишер |
| Гидроксипролин | Hyp, hP | 1902 | Желатин | Э. Фишер |
| Триптофан | Trp, W | 1902 | Казеин | Ф. Гопкинс, Д. Кол |
| Изолейцин | Ile, I | 1904 | Фибрин | Ф. Эрлих |
| Метионин | Met, M | 1922 | Казеин | Герман Джозеф Мёллер |
| Треонин | Thr, T | 1925 | Белки овса | С. Шрайвер и др. |
| Гидроксилизин | Hyl, hK | 1925 | Белки рыб | С. Шрайвер и др. |
Более подробно об аминокислотах читайте в литературе:
- Майстер А., Биохимия аминокислот, перевод с английского, М., 1961;
- Аминокислотное питание свиней и птицы, М., 1963;
- Борис Ильич Збарский, Илья Иванович Иванов, Сергей Руфович Мардашев, Биологическая химия, 4 изд., Л., 1965;
- Иван Семенович Попов, Аминокислотный состав кормов, 2 изд., М., 1965;
- Обмен аминокислот. Материалы Всесоюзной конференции [13 — 17 окт. 1965], Тбилиси, 1967;
- Вацлав Леонович Кретович, Основы биохимии растений, 4 изд., М., 1964.
- Общая биология. Учебник для 9 — 10 классов средней школы. Под ред. Ю. И. Полянского. Изд. 17-е, перераб. — М.: Просвещение, 1987. — 288с.;
- Аминокислоты, пептиды, белки. Под ред. Ю. В. Митина;
- Садовникова М. С., Беликов В. М. Пути применения аминокислот в промышленности. //Успехи химии. 1978. Т. 47. Вып. 2. С. 357?383.
Комментарии к статье
Внимание! Реклама, сквернословие, спам и пр. не по теме статьи удаляется.
Для размещения рекламы обратитесь к администрации сайта.
Нажимая на кнопку "Отправить", я даю согласие на обработку персональных данных